Proteine der Photolyase/Cryptochrom-Proteinfamilie zeigen nach Photoanregung aus dem volloxidierten Zustand ihres Flavin-Kofaktors eine Elektronentransfer-Reaktion, die über eine Kette von drei Tryptophanen abläuft und zu einem mit der zeitaufgelösten EPR detektierbaren Radikalpaarzustand führt.
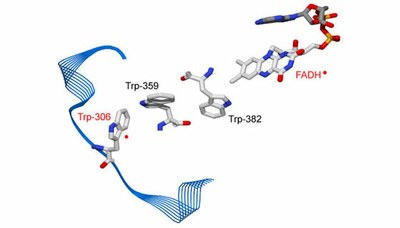
Abbildung: Tryptophan-Kette in Escherichia coli CPD-Photolyase, die am Elektronentransport vom Trp-306 zum Flavin (FAD) beteiligt ist. Rot markiert sind hier die beiden Partner des Radikalpaars, das an der Proteinoberfläche gelegene terminale Tryptophan (Trp-306) und der im Protein verborgene Flavin-Kofaktor (FAD).
Zur theoretischen Beschreibung der EPR-Signale dieser Radikalpaare findet die Theorie gekoppelter Radikalpaare (CCRP) Anwendung.
Literatur
- S. Weber
Light-driven enzymatic catalysis of DNA repair: a review of recent biophysical studies on photolyase
Biochimica et Biophysica Acta (Bioenergetics) 1707 (2005) 1-23.
- C.W.M. Kay, H. Mögling, E. Schleicher, K. Hitomi, K. Möbius, T. Todo, A. Bacher, G. Richter, S. Weber
A comparative time-resolved electron paramagnetic resonance study of the flavin cofactor photoreduction in Escherichia coli cyclobutane pyrimidine dimer photolyase and Xenopus laevis photolyase
Flavins and Flavoproteins 2002 (S. Chapman, R. Perham, N. Scrutton, Editors), Rudolf Weber Agency for Scientific Publishing, Berlin (2002) 713-718.
- S. Weber, C.W.M. Kay, H. Mögling, K. Möbius, K. Hitomi, T. Todo
Photoactivation of the flavin cofactor in Xenopus laevis (6-4) photolyase: observation of a transient tyrosyl radical by time-resolved electron paramagnetic resonance
Proceedings of the National Academy of Sciences USA 99 (2002) 1319-1323.